单选题
一、选择题(每小题只有一个正确答案,每小题3分,10小题共30分)
8
下列符合化学实验“绿色化”的有:
① 在萃取操作的演示实验中,将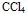 萃取溴水改为
萃取溴水改为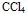 萃取碘水
萃取碘水
② 在铜和浓硝酸反应的实验中,将铜片改为可调节高度的铜丝
③ 将实验室的废酸液和废碱液中和后再排放
① 在萃取操作的演示实验中,将
② 在铜和浓硝酸反应的实验中,将铜片改为可调节高度的铜丝
③ 将实验室的废酸液和废碱液中和后再排放
分值: 3.0分查看题目解析 >
10
下列实验操作完全正确的是
| 编号 | 实验 | 操作 |
| A | 钠与水反应 | 用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
| B | 配制一定浓度的氯化钾溶液1000mL | 准确称取氯化钾固体,放入到1000ml的容量瓶中,加水溶解,振荡摇匀,定容 |
| C | 排除碱式滴定管尖嘴部分的气泡 | 将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出 |
| D | 取出分液漏斗中所需的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
分值: 3.0分查看题目解析 >
问答题
三、(本题包括3小题,共29分)
22
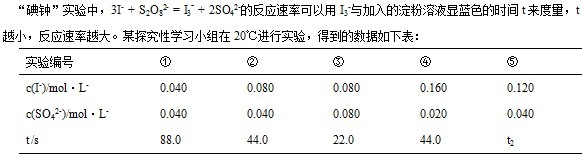
回答下列问题:
(1)该实验的目的是______________________________________________________________。
(2)显色时间t2=________________________ .
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为________________(填字母)
A、<22.0s B、22.0~44.0s C、>44.0s D、数据不足,无法判断
回答下列问题:
(1)该实验的目的是______________________________________________________________。
(2)显色时间t2=________________________ .
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为________________(填字母)
A、<22.0s B、22.0~44.0s C、>44.0s D、数据不足,无法判断
分值: 8.0分查看题目解析 >
23
已知某混合金属粉末,除铝处还含有铁、铜中的一种或两种,所含金属的量都在5%以上。请设计合理实验探究该混合物金属粉末中铁、铜元素的存在。
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1mol/L硫酸、2mol/L硝酸、2mol/LNaOH溶液、20%KSCN溶液。
完成以下实验探究过程:
(1)提出假设:
假设1 该混合金属粉末中除铝外还含有_______元素;
假设2 该混合金属粉末中除铝外还含有_______元素;
假设1 该混合金属粉末中除铝外还含有Fe、Cu元素;
(2)设计实验方案
基于假设3,设计出实验方案(不要在答题卡上作答)。
(3)实验过程
根据(2)的实验方案,叙述实验操作、预期现象和结论。
【提示】Ⅰ.在答题卡上按以下方式作答,注意前后内容对应;
Ⅱ.注意文字简洁,确保不超过答题卡空间。
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1mol/L硫酸、2mol/L硝酸、2mol/LNaOH溶液、20%KSCN溶液。
完成以下实验探究过程:
(1)提出假设:
假设1 该混合金属粉末中除铝外还含有_______元素;
假设2 该混合金属粉末中除铝外还含有_______元素;
假设1 该混合金属粉末中除铝外还含有Fe、Cu元素;
(2)设计实验方案
基于假设3,设计出实验方案(不要在答题卡上作答)。
(3)实验过程
根据(2)的实验方案,叙述实验操作、预期现象和结论。
【提示】Ⅰ.在答题卡上按以下方式作答,注意前后内容对应;
Ⅱ.注意文字简洁,确保不超过答题卡空间。
| 编号 | 实验操作 | 预期现象和结论 |
| ① | ||
| ② | ||
| ③ | ||
| ④ | ||
分值: 11.0分查看题目解析 >
问答题
四、(本题包括3小题,共32分)
26
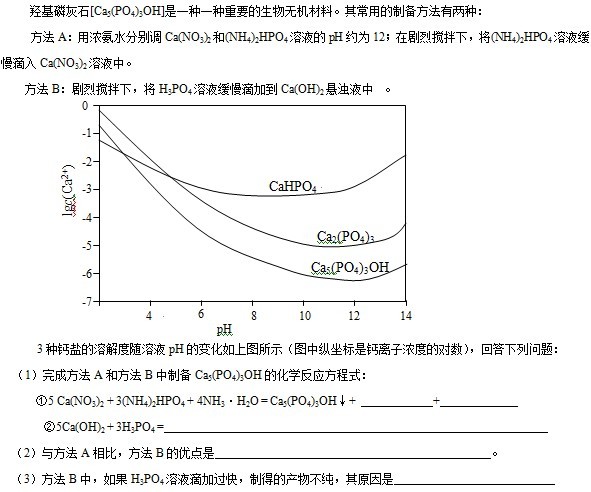
_______________________________________________________________________________
(4)图中所示3种钙盐在人体中最稳定的存在形式是______________(填化学式)。
(5)糖沾附在牙齿上,在酶的作用下产生酸性物质,易造成龋齿。结合化学平衡移动原理,分析其原因 _____________________________________________________________________________。
_______________________________________________________________________________
(4)图中所示3种钙盐在人体中最稳定的存在形式是______________(填化学式)。
(5)糖沾附在牙齿上,在酶的作用下产生酸性物质,易造成龋齿。结合化学平衡移动原理,分析其原因 _____________________________________________________________________________。
分值: 12.0分查看题目解析 >
问答题
五、(本题包括1小题,9分)
27
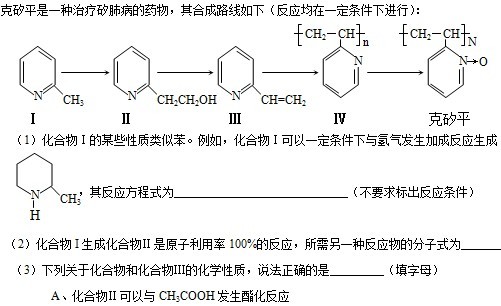
B、化合物Ⅱ不可以与金属钠生成氢气
C、化合物Ⅲ可以使溴的四氯化碳溶液褪色
D、化合物Ⅲ不可以使酸性高锰酸钾溶液褪色
(4)化合物Ⅲ生成化合物Ⅳ的反应方程式为_____________________________(不要求标出反应条件) (5)用氧化剂氧化化合物Ⅳ生成克矽平和水,则该氧化剂为________________________。
B、化合物Ⅱ不可以与金属钠生成氢气
C、化合物Ⅲ可以使溴的四氯化碳溶液褪色
D、化合物Ⅲ不可以使酸性高锰酸钾溶液褪色
(4)化合物Ⅲ生成化合物Ⅳ的反应方程式为_____________________________(不要求标出反应条件) (5)用氧化剂氧化化合物Ⅳ生成克矽平和水,则该氧化剂为________________________。
分值: 9.0分查看题目解析 >
问答题
六、选做题(本题包括2小题,每小题10分,考生只能选做一题。28小题为“有机化学基础”内容的试题,29题为“物质结构与性质”内容的试题)
28
已知苯甲醛在一定条件下可以通过Perkin反应生成肉桂酸(产率45~50%),另一个产物A也呈酸性,反应方程式如下:
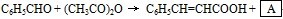
苯甲醛 肉桂酸
(1)Perkin反应合成肉桂酸的反应式中,反应物的物质的量之比为1 :1。产物A的名称是_____________。
(2)一定条件下,肉桂酸与乙醇反应生成香料肉桂酸乙酯,其反应方程式为__________________________
(不要求标出反应条件)
(3)取代苯甲醛也能发生Perkin反应,相应产物的产率如下:
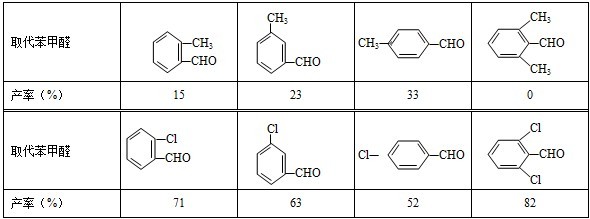
可见,取代基对Perkin反应的影响有(写出3条即可):
①___________________________________________________________________
②___________________________________________________________________
③___________________________________________________________________
(4)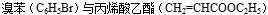 在氯化钯催化下可直接合成肉桂酸乙酯,该反应属于Beck反应,是芳香环上的一种取代反应,其反应方程式为
在氯化钯催化下可直接合成肉桂酸乙酯,该反应属于Beck反应,是芳香环上的一种取代反应,其反应方程式为
______________________________________________(不要求标出反应条件)
(5)Beck反应中,为了促进反应的进行,通常可加入一种显____________(填字母)的物质
A、弱酸性 B、弱碱性 C、中性 D、强酸性
苯甲醛 肉桂酸
(1)Perkin反应合成肉桂酸的反应式中,反应物的物质的量之比为1 :1。产物A的名称是_____________。
(2)一定条件下,肉桂酸与乙醇反应生成香料肉桂酸乙酯,其反应方程式为__________________________
(不要求标出反应条件)
(3)取代苯甲醛也能发生Perkin反应,相应产物的产率如下:
可见,取代基对Perkin反应的影响有(写出3条即可):
①___________________________________________________________________
②___________________________________________________________________
③___________________________________________________________________
(4)
______________________________________________(不要求标出反应条件)
(5)Beck反应中,为了促进反应的进行,通常可加入一种显____________(填字母)的物质
A、弱酸性 B、弱碱性 C、中性 D、强酸性
分值: 10.0分查看题目解析 >